当医生开出包含四种药物的治疗方案时,许多患者会感到困惑:为什么要用这么多药?它们如何协同作用?漏服一种会怎样?事实上,四联用药是临床针对复杂疾病的重要策略,尤其在幽门螺杆菌感染、慢性心衰等疾病中,其科学性和必要性已被大量研究证实。本文将从实际案例出发,解析四联用药的作用机制、优化策略及注意事项,帮助公众科学理解这一治疗手段。
四联用药的核心在于通过不同机制药物的协同作用,实现对疾病的多维度控制。以幽门螺杆菌感染为例,其治疗方案通常包含质子泵抑制剂(抑制胃酸)、铋剂(保护胃黏膜)及两种抗生素(杀菌)。四类药物分工明确:
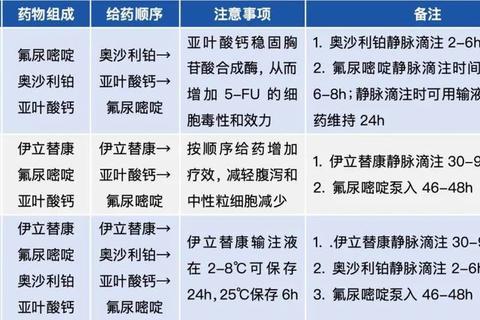
1. 抑酸剂(如雷贝拉唑)通过提高胃内pH值,为抗生素创造稳定的杀菌环境[[60][66]];
2. 铋剂(如枸橼酸铋钾)覆盖溃疡创面,减少胃酸刺激[[60][66]];
3. 抗生素组合(如阿莫西林+克拉霉素)针对不同耐药机制,降低治疗失败风险[[60][31]]。
研究表明,四联疗法的根除率可达90%以上,显著高于传统三联方案[[66][31]]。类似原理也应用于心衰治疗,通过ARNI、β受体阻滞剂、MRA和SGLT2i的联合,从改善血流动力学、抑制神经内分泌激活等多角度延缓疾病进展。
不同患者的生理状态、耐药性及合并症差异显著。例如:
四联用药常见副作用包括恶心、腹泻、头痛等,通常轻微且可逆。优化策略包括:
幽门螺杆菌感染患儿需调整抗生素剂量(按体重计算),并避免使用可能影响骨骼发育的喹诺酮类。
多数四联药物可能通过胎盘或乳汁影响胎儿,需严格评估风险。例如,铋剂和部分抗生素(如克拉霉素)在妊娠早期禁用[[60][65]]。
幽门螺杆菌治疗需完成14天疗程,擅自停药易导致耐药菌株残留[[60][78]]。
不同药物组合的抗菌谱和相互作用差异显著。例如,含克拉霉素的方案与某些降压药联用可能引发QT间期延长。
1. 规范用药记录:使用手机提醒或分药盒,避免漏服、错服;
2. 饮食配合:治疗期间忌烟酒、辛辣食物,减少胃黏膜刺激;
3. 复查与随访:疗程结束后4-8周复查(如C13呼气试验),确认根除效果[[31][66]]。
随着基因检测和耐药性快速筛查技术的普及,个体化四联方案将成为趋势。例如,通过检测幽门螺杆菌的CYP2C19基因型,可预测患者对质子泵抑制剂的代谢速度,从而调整剂量。新型抑酸剂(如凯普拉生)的上市,为耐药患者提供了更优选择。
四联用药是医学进步的体现,但其成功依赖于医患双方的密切配合。患者需充分信任医生方案,严格遵循用药指导;医生则需动态评估疗效与风险,及时调整策略。唯有如此,才能在对抗复杂疾病的道路上走得更稳、更远。