肺纤维化曾被视为“不治之症”,患者肺部逐渐被瘢痕组织取代,呼吸如同被束缚般艰难。一位57岁的患者李女士,因长期干咳未重视,最终确诊时肺部已形成“蜂窝肺”,肺功能仅剩正常人的40%。如今,随着靶向药物和新型治疗策略的突破,这类患者终于迎来转机——全球首个针对病理成纤维细胞转化的药物进入临床试验,中国患者更是同步用上了国际创新药。
肺纤维化的本质是成纤维细胞异常活化,导致细胞外基质过度沉积。近年研究发现,LEPR+成纤维细胞在肺泡区域异常增殖,并在RUNX2转录因子驱动下转化为分泌胶原蛋白的“病理成纤维细胞”。这一过程涉及多个关键环节:
1. 病理细胞起源:肺泡成纤维细胞在损伤刺激(如博莱霉素、矽尘)下发生表型转化,αSMA和CTHRC1蛋白表达激增,形成不可逆的纤维化病灶。
2. 信号通路异常:TGF-β、PDGF等促纤维化因子激活,同时RUNX2通过调控Cthrc1等基因,加剧胶原沉积。
3. 微环境改变:成纤维细胞与免疫细胞(如巨噬细胞)相互作用,形成促纤维化微循环。
> 科学图解:病理成纤维细胞转化过程中,RUNX2基因的染色质可及性显著增加,其结合位点富集在促纤维化基因启动子区域。

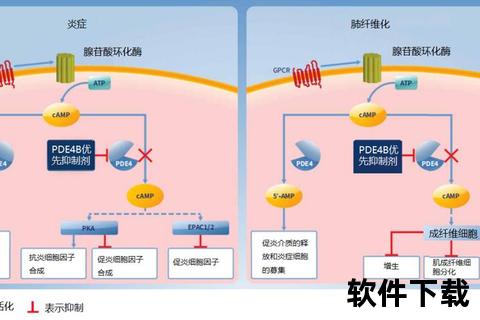
勃林格殷格翰的nerandomilast(PDE4B抑制剂)在III期试验中实现十年来首次显著改善肺功能,预计2026年上市。其优势在于选择性抑制肺部高表达的PDE4B亚型,呕吐等副作用较传统药物减少50%。
> 药物对比:尼达尼布对早期纤维化效果更佳,而PDE4B抑制剂可能更适合晚期患者。临床建议根据肺功能指标(如FVC)个体化选择。
突发呼吸困难或血氧饱和度低于90%时:
2025年《自然》子刊报道,通过多组学分析锁定ANO9、FAM13A等6个新靶点,其中FAM13A基因变异者对尼达尼布响应率提高3倍。人工智能预测模型已能根据基因谱系推荐最优药物组合,精准治疗时代即将到来。
> 专家提醒:肺纤维化治疗需“三早原则”——早发现、早诊断、早用药。现有药物虽不能完全逆转纤维化,但规范治疗可使5年生存率从30%提升至60%。
行动建议
1. 40岁以上长期咳嗽人群,建议每年做肺功能检测
2. 确诊患者优先选择纳入医保的尼达尼布(月均费用约1200元)
3. 参与临床试验(如PFF社区注册项目)可优先获得创新疗法
(本文所述治疗方案需在专业医师指导下实施)