“每次吃药都像在胃里点了一把火”,这是一位慢性十二指肠溃疡患者的真实。传统口服药物常因胃酸破坏或肠道吸收不均导致疗效不足,而频繁的服药和副作用更让患者苦不堪言。随着医学技术的进步,一种名为“十二指肠靶向给药系统”的创新方案逐渐走入大众视野。它像一枚智能导航导弹,将药物精准送达病灶部位,减少全身副作用,提升疗效——这不仅是一次技术突破,更是患者生活质量的重大改善。
一、为何需要十二指肠靶向给药?
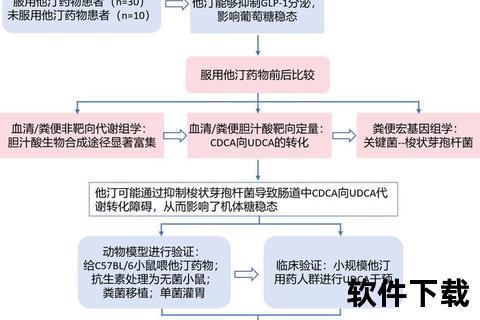
1. 十二指肠的生理挑战
十二指肠是消化系统的重要枢纽,承担着消化液分泌和营养吸收的关键功能。其酸性环境(pH 1.5-3.5)、频繁蠕动及酶解作用,使传统药物在此处面临三大难题:
药物降解:胃酸和胰酶破坏药物结构(如蛋白质类药物);
吸收不均:药物在短时间(1-2小时)内快速通过,难以有效吸收;
局部刺激:药物释放过早可能损伤胃黏膜,引发恶心、溃疡等副作用。
2. 临床需求驱动创新
十二指肠疾病种类繁多,包括溃疡、炎症、肿瘤及代谢性疾病(如糖尿病)。例如,糖尿病患者需长期服用肠促胰岛素类药物(如GLP-1类似物),但其易被胃酸破坏,需频繁注射。靶向给药系统可突破这一困境,实现口服替代。
二、靶向给药的核心技术:突破胃肠屏障
1. 物理屏障的智能跨越
pH响应系统:利用十二指肠碱性环境(pH 6.0-7.4)触发药物释放。例如,肠溶包衣材料(如Eudragit®)在胃酸中保持稳定,进入十二指肠后溶解。
时间控制释放:通过缓释技术(如渗透泵系统)延长药物在十二指肠的停留时间,匹配肠道转运节律。
2. 生物相容性载体技术
纳米载体:脂质体、聚合物纳米粒等可保护药物免受酶解,并通过细胞旁路或主动转运穿透肠黏膜。
外泌体递送:天然来源的外泌体具有低免疫原性和高效靶向性,可携带药物穿越生物屏障,已在糖尿病和肿瘤治疗中展现潜力。
3. 靶向分子的精准识别
受体介导:如维生素B12受体在十二指肠高表达,可设计受体结合型载体实现定向富集;
抗体/肽段标记:针对疾病标志物(如炎症因子)设计抗体偶联载体,提升病灶靶向性。
三、临床应用:从理论到实践
1. 炎症与溃疡治疗
案例1:布地奈德(糖皮质激素)的结肠靶向制剂已被用于炎症性肠病,类似技术可调整至十二指肠,用于嗜酸性粒细胞性十二指肠炎,减少全身激素暴露。
案例2:铋剂(如枸橼酸铋钾)通过纳米载体靶向十二指肠溃疡部位,加速黏膜修复,减少铋剂在肾脏的蓄积风险。
2. 代谢性疾病管理
口服胰岛素:基于pH响应纳米粒的胰岛素制剂已在动物实验中实现血糖控制,未来有望替代注射。
GLP-1类似物:外泌体包裹的GLP-1可抵抗酶解,延长半衰期,改善糖尿病患者依从性。
3. 肿瘤精准治疗
化疗药物:紫杉醇脂质体通过靶向十二指肠肿瘤血管,减少抑制和脱发等副作用。
免疫调节剂:局部递送PD-1抑制剂至十二指肠肿瘤微环境,增强抗肿瘤免疫应答。
四、患者指南:如何判断是否需要靶向治疗?
1. 适用人群
慢性十二指肠溃疡反复发作者;
需长期服用胃肠刺激性药物(如非甾体抗炎药);
代谢性疾病患者(如糖尿病、肥胖)需替代注射治疗;
对传统药物耐受性差或疗效不足者。
2. 就医信号
紧急情况:呕血、黑便、剧烈腹痛——立即急诊;
常规就诊:持续上腹灼痛、餐后腹胀、体重下降——需胃肠镜评估。
3. 特殊人群注意事项
儿童:优先选择口感佳、剂量灵活的剂型(如口腔崩解片);
孕妇:避免使用含磁性纳米粒的靶向系统(潜在发育风险);
老年人:选择缓释制剂减少服药频率,避免漏服。
五、未来展望与日常建议
1. 技术趋势
3D打印个性化制剂:根据患者肠道形态定制药物形状和释放曲线;
微生物疗法:工程化益生菌携带药物定植十二指肠,实现持续释放。
2. 患者日常管理
饮食配合:高纤维饮食延缓胃排空,增加靶向药物作用时间;
用药依从性:定时服药,避免与抑酸药(如奥美拉唑)同时使用;
症状监测:记录疼痛频率、大便性状,定期复查内镜。
十二指肠靶向给药系统不仅是技术的革新,更是医学人文关怀的体现。它让治疗从“粗放式轰炸”转向“精准化修复”,让患者告别频繁用药的痛苦,重获健康生活的掌控权。未来,随着更多创新技术的落地,这种“直击病灶”的治疗模式或将成为慢性胃肠疾病管理的金标准。
