当我们的喉咙开始刺痛、体温逐渐攀升,或是皮肤出现红肿热痛时,医生常常会开出一盒名为“阿莫西林”的药物。这种白色小药片为何能对抗感染?它的抗菌机制背后隐藏着怎样的科学智慧?我们将在下文中揭开β-内酰胺类药物与细菌细胞壁之间的生死博弈。
细菌感染的本质,是致病菌在人体内大量繁殖并释放毒素的过程。这些直径仅0.5-5微米的微生物,通过细胞壁构筑起坚固的防御工事。这层由肽聚糖交织而成的网状结构,既能维持细菌形态,又能抵抗体内渗透压差异带来的压力,堪称细菌存活的“生命铠甲”。
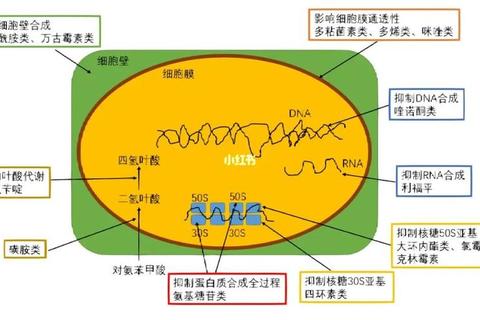
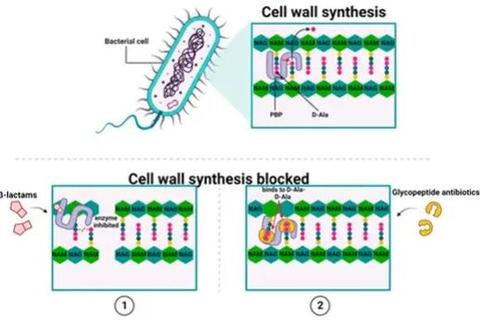
阿莫西林作为β-内酰胺类抗生素的代表,其核心作用机制正是精准破坏这一关键结构。它通过模仿细菌细胞壁合成所需的“建筑材料”——D-丙氨酰-D-丙氨酸分子结构,诱骗细菌将其摄入体内。当阿莫西林与细菌细胞膜上的青霉素结合蛋白(PBPs)结合后,会永久性阻断肽聚糖链的交联反应,导致细胞壁出现致命缺口。
这种作用方式类似于在城墙的关键接合处插入一枚楔子。随着细菌持续分裂增殖,缺损的细胞壁无法承受内部高压,最终导致菌体膨胀破裂。值得注意的是,这一过程具有高度选择性——人体细胞没有细胞壁结构,因此阿莫西林对宿主细胞的损伤极小。
阿莫西林的广谱抗菌特性源于其对不同细菌PBPs的识别能力:
但这种广谱性也带来挑战。约30%的耐药菌株通过产生β-内酰胺酶分解药物,或通过改变PBPs结构逃避结合。临床常采用“阿莫西林+克拉维酸钾”的复方制剂,利用β-内酰胺酶抑制剂提升疗效。
1. 精准识别适应症
适用于中耳炎、肺炎、皮肤感染等细菌感染,但对病毒性感冒、手足口病等无效。当出现持续高热(>3天)、脓性分泌物、血象升高等细菌感染征象时使用。
2. 特殊人群用药警示
3. 规范用药行为
全球每年约70万人死于耐药菌感染,这个数字可能在2050年突破千万。阿莫西林作为基层医疗的“守门员”,其有效性正面临严峻挑战。普通民众可通过以下方式守护抗生素疗效:
当出现反复感染、常规治疗无效时,应及时进行细菌培养+药敏试验。这项不足百元的检测,能帮助医生精准选择抗菌药物,避免经验性用药的盲目性。
在微生物与人类长达百万年的博弈中,阿莫西林等抗生素的诞生曾让我们占据上风。但这场战争的最终胜利,不仅依赖药物的更新迭代,更需要每个用药者保持敬畏之心。记住:每一次规范用药,都是在为人类保留对抗疾病的终极武器。